Задача 16. Определение структуры с учетом
стереохимии
Задача 17. Спектроскопия ЯМР и определение
структуры органических веществ
Задача 18. Синтез полимеров
Задача 19. Органический синтез с элементами
региоселективности
Задача 20. Карбоновые кислоты
Задача 16. Определение структуры с учетом стереохимии
Кислый вкус плодов цитрусовых в основном обусловлен лимонной (2-гидрокси-1,2,3-пропантрикарбоновой) кислотой. Коммерческое производство лимонной кислоты основано на ферментации мелассы или крахмала с помощью грибка Aspergillus niger при pH 3.5. Эта кислота широко применяется в пищевой промышленности при изготовлении безалкогольных напитков и в качестве протравы при крашении. Она также является важным промежуточным соединением в биохимии.
а. Что произойдет с лимонной кислотой при нагревании до 45-50o С с концентрированной серной кислотой? Приведите структуру полученного продукта и его название по номенклатуре ИЮПАК. Какой тип органических кислот вступает в подобную реакцию?
После нагревания лимонной кислоты с серной кислотой, к реакционной смеси добавили анизол (метоксибензол) и получили продукт А (C12H12O5).
б. Установите структуру вещества А.
в. Определите возможные изомеры А в этой
реакции и приведите их структуры, абсолютные
конфигурации и названия по номенклатуре ИЮПАК.
г. Сколько стереоизомеров вещества А
будет получено в реакции бромирования?
Изобразите их фишеровские проекции.
д. Укажите абсолютную конфигурацию всех
стереоцентров во всех стереоизомерах, указанных
в предыдущем задании г.
Если вместо анизола в реакционную смесь добавлять фенол или резорцин, то образуются соответственно продукты В и С. Вещество В, в отличие от С, не дает окрашивания с нейтральным раствором FeCl3. При одинаковых условиях проведения реакции выход вещества С значительно выше, чем выход В.
е. Приведите структуры веществ В и С.
ж. В чем разница между реакциями, приводящими
к образованию А и В?
з. Почему выход вещества С выше, чем выход В?
Задача 17. Спектроскопия ЯМР и определение структуры органических веществ
При идентификации двух веществ А и В были получены следующие результаты.
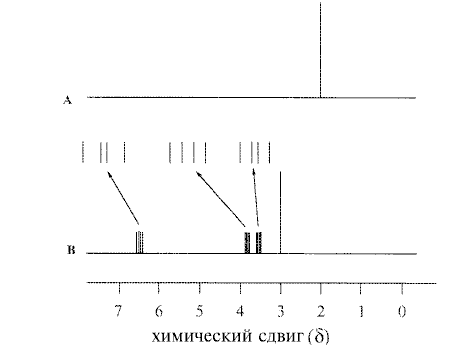
Оба вещества имеют молекулярную формулу C3Н6О. Ниже приведены схематические 1Н-ЯМР спектры этих веществ при 400 МГц. Положение и относительная интенсивность разных линий в 1Н-ЯМР спектре вещества В приведены в Таблице (Примечание: для облегчения анализа значения несколько изменены по сравнению с экспериментальными данными).

Схемы 1H-ЯМР спектров веществ А и В при 400 МГц
Положения и относительные
интенсивности индивидуальных линий
в 1Н-ЯМР спектре (400 МГц) вещества В
Линия |
Положение (м.д.) |
Относительная интенсивность |
1 |
6.535 |
1 |
2 |
6.505 |
1 |
3 |
6.495 |
1 |
4 |
6.465 |
1 |
5 |
3.930 |
1 |
6 |
3.910 |
1 |
7 |
3.890 |
1 |
8 |
3.870 |
1 |
9 |
3.525 |
1 |
10 |
3.505 |
1 |
11 |
3.495 |
1 |
12 |
3.475 |
1 |
13 |
3.000 |
12 |
Одно из этих веществ реагирует с малоновой
кислотой с образованием вещества, известного как
кислота Мелдрама (С6Н8О4), в 1Н-ЯМР
спектре которого имеются линии между 0 и 7.0 ![]() . ИК спектр имеет пик в области
1700-1800 см-1. В присутствии основания это
вещество конденсируется с ароматическим
альдегидом.
. ИК спектр имеет пик в области
1700-1800 см-1. В присутствии основания это
вещество конденсируется с ароматическим
альдегидом.
а. Используя ЯМР спектры, приведенные на рисунке, определите неизвестные вещества и назовите их по номенклатуре ИЮПАК.
б. В 1Н-ЯМР спектре вещества В припишите позиции пиков конкретным протонам.
в. Рассчитайте константы спин-спинового взаимодействия протонов вещества В.
г. Переведите положения первых четырех линий в Гц (в соответствии с таблицей). Какими были бы позиции пиков этих линий в Гц, если бы спектр снимали при 600 МГц?
д. Изобразите возможную структуру кислоты Мелдрама.
е. Кислота Мелдрама имеет рКа = 4.83. Объясните ее кислотные свойства.
ж. Приведите структуру продукта конденсации кислоты Мелдрама с ароматическим альдегидом.
Задача 18. Синтез полимеров
Этилен находит все новые применения в крупнотоннажном производстве химических веществ, в частности полимеров. Громадные количества его получают термическим и каталитическим крекингом алканов, выделяемых из природного газа и нефти.
В присутствии серебряного катализатора этилен реагирует с кислородом, образуя Р. Соединение Р при нагревании с подкисленной водой образует Q. 1Н-ЯМР спектр вещества Р имеет только один сигнал, тогда как спектр Q содержит два сигнала.
а. Идентифицируйте вещества Р и Q и изобразите их структуры.
При взаимодействии Р и Q образуется вещество R. Оно реагирует с SOCl2 с образованием вещества S. При нагревании со спиртовым раствором KOH S образует Т, вещество с анестезирующими свойствами, называемое "винэтен".
| SOCl2 | KOH | |||||
| P | +Q |
|
R |
|
S | |
| спирт |
б. Определите вещества R, S и T.
Другое вещество, диметилбензол-1,4-бис(ацетат), может быть синтезировано из п-ксилола. Для того, чтобы получить нужные промежуточные соединения и конечный продукт, в этом синтезе нужно использовать соответствующие реагенты. Ниже приведены структуры промежуточных продуктов в синтезе диметилбензол-1,4-бис(ацетата):
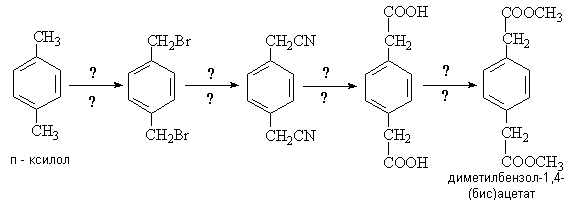
в. Идентифицируйте реагенты, использованные
в синтезе диметилбензол-1,4-бис(ацетата).
г. Сколько пиков, по вашему мнению, содержит 1Н-ЯМР
спектр диметилбензол-1,4-бис
(ацетата)?
При нагревании смеси диметилбензол-1,4-бис(ацетата)
и вещества R (полученного из этилена)
образуется полимер. д. Изобразите структуру
полимера.
е. Что произойдет при обработке полимера
1. КОН(водн) (нагревание), затем H+/H2O?
2. LiAlH4?
ж. Избыток диметилбензол-1,4-бис(ацетата) был случайно нагрет с глицерином, и это привело к образованию другого полимера. Какова вероятная структура этого полимера? Пригоден ли он для вытягивания волокон?
Задача 19. Органический синтез с элементами региоселективности
Получение заданных дизамещенных производных бензола из монозамещенных бензолов реакцией электрофильного замещения - одна из трудных проблем органического синтеза. Элегантным решением этой проблемы является описанный ниже синтез анальгетика - лекарственного препарата Трамадол (C16H25NO2). Первая стадия этого синтеза:
| HSbF6 | ||
| Фенол |
|
А |
| галоген |
В масс-спектре вещества А в области максимальных значений отношения m/z имеются два пика равной интенсивности при 172 и 174. При нитровании в мягких условиях А дает смесь трех изомерных мононитропроизводных.
а. Изобразите структуру вещества А. В чем проявляется региоселективность в реакции превращения фенола в А? Объясните значение этой реакции.
Рассмотрите следующую реакцию:
| (CH3)2SO4 / NaOH | Mg / ТГФ / толуол | |||
А |
|
В |
|
С |
В области максимальных значений отношения m/z масс-спектра вещества В присутствуют пики равной интенсивности при 186 и 188.
б. Приведите структуры соединений В и С. Как изменяется реакционная способность соединения после превращения В в С?
Еще одно промежуточное соединение D, необходимое для синтеза Трамадола, получают следующим образом:
параформ |
||
| Циклогексанон |
|
D (C9H17NO)(растворим в HCl) |
| диметиламин | ||
гидролиз |
||
| C + D |
|
Трамадол |
в
Задача 20. Карбоновые кислоты
Кетоэфиры - это высокореакционноспособные бифункциональные вещества; они находят применение в синтезе алифатических и гетероциклических соединений.
а. Молекулярной формуле С5Н8О3 соответствуют два изомерных кетоэфира X и Y. Изобразите их возможные структуры.
Каждый из этих сложных эфиров сначала вводят в
реакцию с бензилбромидом в присутствии CH3ONa,
затем образовавшиеся продукты обрабатывают
одним или двумя эквивалентами сильного
основания, например, диизопропиламидом лития
(ЛДА), после этого - одним эквивалентом CH3I.
Полученные продукты гидролизуют водным
раствором HCl.
в. Конечный продукт, полученный после
завершения реакций из кетоэфира X, является
нейтральным веществом (молекулярная формула C11H14O),
тогда как кетоэфир Y образует кетокислоту
(молекулярная формула C12H14O3).
Дайте объяснение этому факту.
г. Кетоэфир X образует различные
продукты в зависимости от количества ЛДА,
введенного в реакцию. Объясните, что происходит,
когда:
1. в реакцию вводится один эквивалент ЛДА;
2. в реакцию вводятся два эквивалента ЛДА.